Per i team biofarmaceutici, scegliere tra BFS e FFS non è più solo una decisione di confezionamento; si tratta di una decisione di *gestione del rischio* che influisce direttamente sulla sicurezza del paziente, sulla resa dei lotti e sulla fiducia normativa. Dalla mia esperienza di lavoro con CDMO e stabilimenti farmaceutici in Asia ed Europa, i progetti di maggior successo sono quelli che allineano il sistema di chiusura contenitore con il *profilo di sensibilità termica* del biologico e la tolleranza al rischio di contaminazione del mercato di riferimento. [vxpbiologics ]
In questo articolo, confronteremo BFS e FFS attraverso la lente della garanzia asettica, dei percorsi di contaminazione e dell'implementazione nel mondo reale per i prodotti biologici termolabili, quindi condivideremo liste di controllo di selezione pratiche e suggerimenti di layout basati su linee BFS/FFS su larga scala simili a quelle fornite da Ningbo Everheal Medical Equipment Co., LTD. [rommelag ]
Principi fondamentali di BFS e FFS nel riempimento-finitura biologico
BFS e FFS integrano entrambi formatura, riempimento e sigillatura in un'unica linea, ma *controllano la contaminazione* in modi molto diversi. Comprendere questi principi fondamentali è essenziale prima di valutare quale protegge meglio le API, le proteine e i vaccini termosensibili. [supporto ]
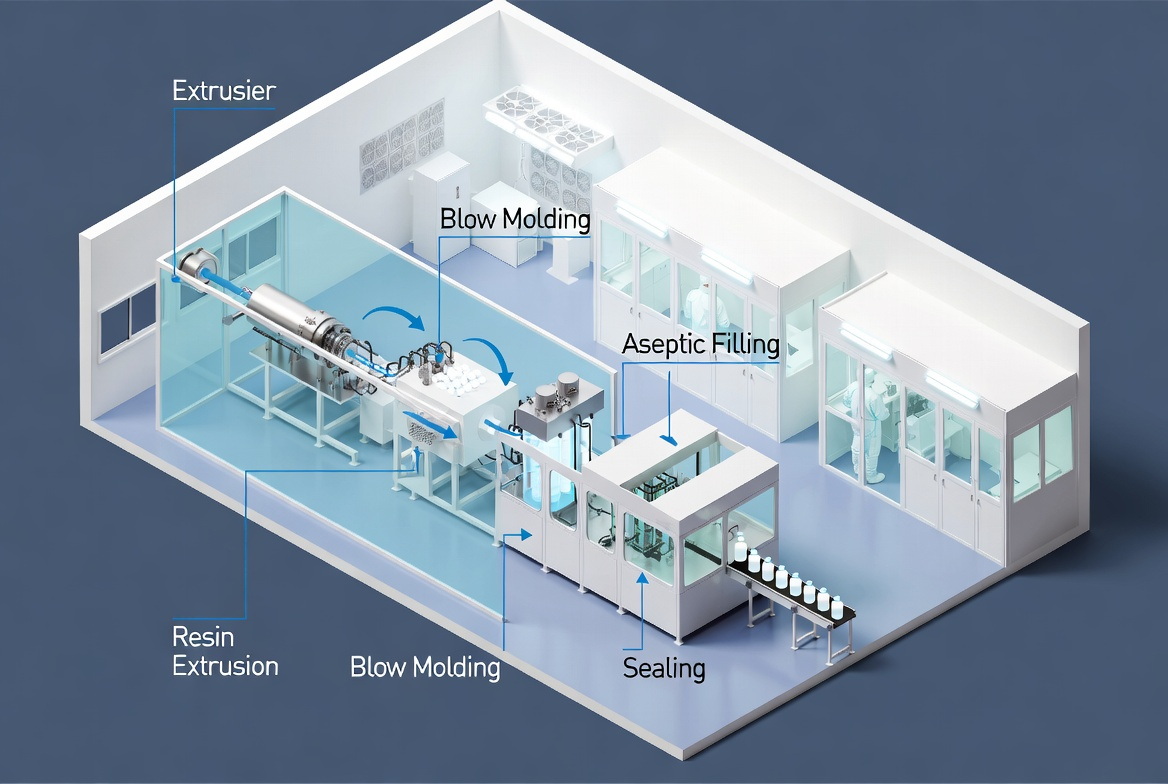
Cos'è il Blow-Fill-Seal (BFS)?
In un sistema BFS, la macchina estrude resina termoplastica fusa (spesso LDPE, HDPE o PP) in un parison caldo, soffia il contenitore, lo riempie con prodotto sterile e lo sigilla in una camera asettica completamente chiusa in un ciclo continuo. Questi cicli generalmente si completano in meno di 20 secondi, il che limita drasticamente il tempo di esposizione ambientale del biologico. Poiché il contenitore viene formato mentre la plastica è ad alta temperatura all'interno di un ambiente controllato, il corpo del contenitore stesso acquisisce un grado di sterilità intrinseca prima del contatto con il prodotto. [apigetto ]
Principali vantaggi asettici del BFS: [linkedin ]
- Sistema chiuso dalla formazione del contenitore fino alla sigillatura, con trasferimento aperto minimo o nullo.
- molto limitato Intervento umano durante le fasi asettiche critiche.
- Elevata ripetibilità del processo grazie alla completa automazione.
- Forte riconoscimento normativo come tecnologia asettica avanzata da parte di autorità come la FDA. [prestocontatto ]
Cos'è il Form-Fill-Seal (FFS)?
In FFS, l'attrezzatura forma confezioni flessibili o semirigide da film di qualità farmaceutica, le riempie di prodotto e le salda a caldo lungo la linea. La pellicola viene svolta, modellata in una busta, bustina o sacchetto, quindi riempita e sigillata, spesso all'interno di un ambiente controllato utilizzando fasi di decontaminazione come il perossido di idrogeno (H₂O₂) o il trattamento con vapore della pellicola o dell'area di formatura. [rommelag ]
Principali caratteristiche asettiche della FFS: [linkedin ]
- Percorso del film più aperto , quindi il materiale può essere esposto all'aria ambiente per distanze e tempi più lunghi.
- Richiede ulteriori passaggi di sterilizzazione e decontaminazione per ottenere un'elevata garanzia asettica (ad es. spray sterilizzanti, flusso d'aria laminare, isolatori).
- Molto flessibile nei formati delle confezioni e adatto per liquidi, polveri e alcuni dispositivi.
Percorsi del rischio di contaminazione: BFS vs. FFS per prodotti biologici termosensibili
Per i prodotti biologici termosensibili, di solito non è possibile fare affidamento sulla sterilizzazione terminale; è invece la fase di riempimento asettico a sostenere il carico del rischio. Ecco perché i percorsi di contaminazione in ogni nodo (aria, superfici, film, operatori) diventano fondamentali quando si confrontano BFS e FFS. [soluzionisteriliwoodstock ]
Profilo di rischio di contaminazione BFS
La BFS è ampiamente considerata come una delle tecnologie a minor rischio per i prodotti liquidi sterili. [linkedin ]
I tipici controlli del rischio di contaminazione in BFS includono: [vxpbiologics ]
- Camera di formatura e riempimento chiusa con aria filtrata HEPA e sovrapressione.
- Contenitore formato e sigillato nella stessa macchina, evitando qualsiasi trasferimento aperto.
- Nessun vetro, quindi nessun rischio di perdita di particelle o rottura.
- Tempo di esposizione ultrabreve (secondi) tra la formazione del contenitore e la sigillatura.
Per i prodotti biologici termosensibili, il BFS offre un grande vantaggio: spesso è possibile evitare la sterilizzazione terminale ad alta temperatura perché l'intero processo è asettico per natura e l'esposizione al calore è per lo più limitata alla parete del contenitore prima del riempimento. Ciò è particolarmente rilevante per le proteine, gli anticorpi monoclonali e alcuni antigeni vaccinali che si degradano rapidamente sotto l’effetto del calore o delle radiazioni. [supporto ]
Profilo di rischio di contaminazione FFS
Al contrario, l’FFS deve gestire i rischi di contaminazione lungo un percorso del film più lungo e aperto. I sistemi FFS farmaceutici avanzati possono raggiungere livelli elevati di sterilità, ma in genere solo se combinati con robuste tecnologie di decontaminazione e barriera . [prestocontatto ]
I comuni controlli della contaminazione nelle linee FFS asettiche includono: [linkedin ]
- continua del film Decontaminazione tramite H₂O₂, UV o vapore.
- RABS o sistemi di isolamento per separare fisicamente gli operatori dalla zona critica.
- rigoroso Monitoraggio ambientale , compreso il conteggio delle particelle vitali e non vitali lungo il percorso della pellicola.
- Attenta gestione delle ganasce e degli ugelli di saldatura , che possono entrare ed uscire dalla zona critica.
Per i prodotti biologici termosensibili, la FFS può essere impegnativa perché le fasi di decontaminazione (ad esempio, superfici calde, sterilizzanti reattivi) non devono mai compromettere i prodotti biologici stessi. È necessaria una meticolosa convalida del processo per dimostrare che lo sterilizzante residuo o il calore non influiscono sulla potenza o sulla stabilità. [supporto ]
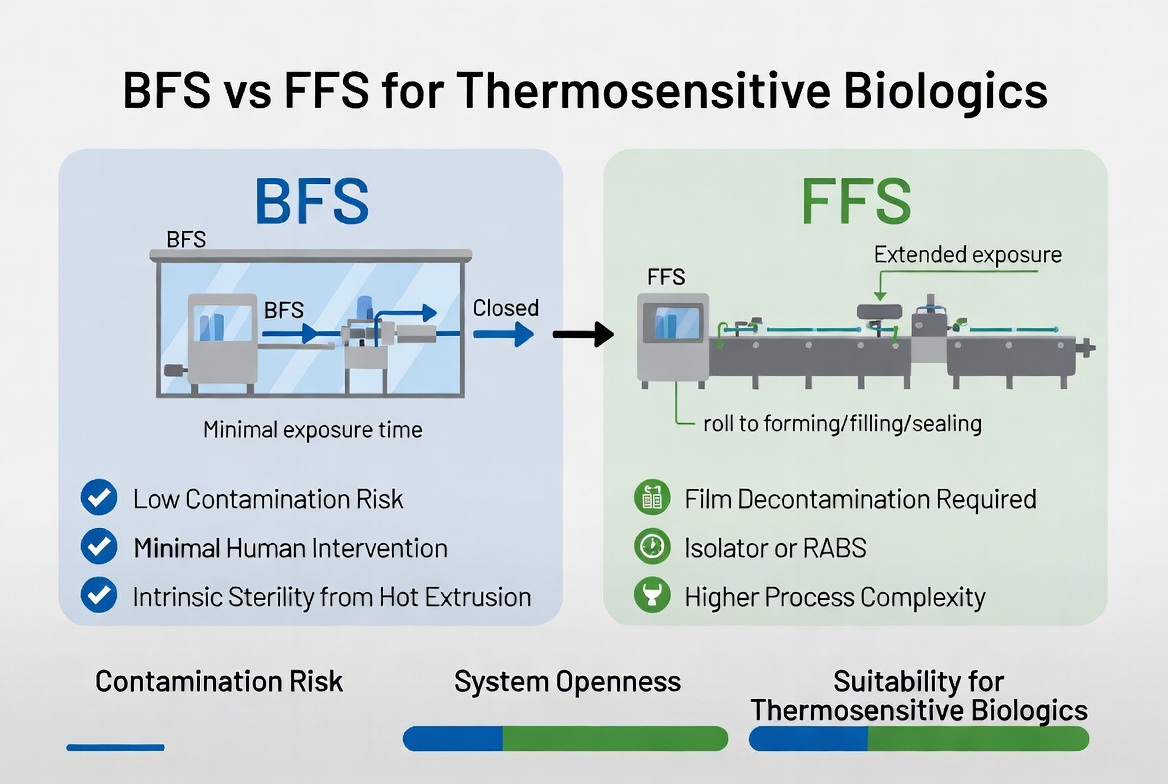
Confronto affiancato di contaminazione e idoneità biologica
La tabella seguente riassume i fattori chiave che contano quando l'obiettivo è ridurre al minimo il rischio di contaminazione per i prodotti biologici termosensibili.
| Fattore |
BFS (Blow-Fill-Seal) |
FFS (Form-Fill-Seal) |
| Materiale del contenitore centrale |
Resina termoplastica (LDPE, HDPE, PP) formata in linea allo stato fuso presto |
Film prefabbricati di qualità farmaceutica, talvolta laminati multistrato presto |
| Apertura del sistema |
Altamente chiuso; formatura, riempimento, sigillatura in una camera asettica chiusa presto |
Percorso cinematografico più aperto; richiede decontaminazione, gestione del flusso d'aria e barriere presto |
| Intervento umano |
Minimo durante le fasi critiche, elevata automazione presto |
Maggiore potenziale di intervento; mitigato da RABS/isolatori e SOP rommelag |
| Tempo di esposizione |
Secondi tra la formazione e il sigillo presto |
Tempi di percorrenza e di permanenza lungo la linea più lunghi presto |
| Rischio di contaminazione tipico |
Tra i più bassi nel riempimento-finitura asettico, forte supporto normativo presto |
Altamente dipendente dal design e dai controlli; il rischio aumenta in caso di scarsa barriera o decontaminazione rommelag |
| Adatto per prodotti biologici termosensibili |
Molto potente, soprattutto laddove la sterilizzazione terminale non è fattibile vxpbiologics |
Possibile, ma richiede un'attenta convalida della pellicola, dello sterilizzante e dell'impatto termico supporto |
| Formati biologici tipici |
Oftalmici, prodotti inalatori, iniettabili, alcuni vaccini vxpbiologics |
Alcune buste biologiche, diluenti, soluzioni sfuse in imballaggi flessibili rommelag |
Prospettiva dell’esperto – Quando BFS è chiaramente leader nel settore dei prodotti biologici termosensibili
Dal punto di vista di un professionista del settore, esistono chiari scenari in cui BFS è la scelta predefinita se si desidera ridurre al minimo il rischio di contaminazione per i prodotti biologici termosensibili. I case report del settore indicano una crescente adozione del BFS per soluzioni oftalmiche prive di conservanti, iniettabili complessi e prodotti biologici per inalazione, proprio perché questi prodotti non possono tollerare regimi di sterilizzazione aggressivi. [soluzionisteriliwoodstock ]
Nelle mie revisioni di progetto con strutture sterili, tre fattori ricorrenti spingono i team verso BFS per prodotti termolabili:
1. Fiducia normativa nella progettazione asettica – Il BFS è descritto nelle linee guida FDA ed EMA come un processo asettico avanzato, che semplifica la giustificazione rispetto ai concetti asettici FFS altamente personalizzati. [apigetto ]
2. Rischio ridotto correlato all'operatore : BFS funziona con pochissimi interventi manuali all'interno della zona critica, riducendo la contaminazione da camici, violazioni dell'integrità dei guanti ed errori umani. [linkedin ]
3. Integrità del contenitore e controllo del particolato – I contenitori polimerici stampati in linea uniformi riducono il rischio di particolato derivante dalla rottura del vetro e dalla frammentazione dei tappi, problemi particolarmente critici per i prodotti iniettabili. [vxpbiologics ]
Per i prodotti biologici con margini di stabilità ristretti, questi fattori spesso superano la ridotta flessibilità del BFS nella progettazione della confezione. [vxpbiologics ]
Dove ha ancora senso una linea FFS ad alte prestazioni
Detto questo, la FFS non viene automaticamente squalificata per i prodotti biologici termosensibili. Diverse grandi aziende farmaceutiche utilizzano con successo sistemi FFS ad alte specifiche per riempire asetticamente soluzioni di aminoacidi, nutrizione parenterale e alcune soluzioni biologiche in sacche flessibili. [rommelag ]
Le situazioni in cui FFS può essere praticabile includono: [linkedin ]
- Il biologico è moderatamente termosensibile ma stabile nell'intervallo termico utilizzato per la sigillatura della pellicola e l'aerazione dello sterilizzante.
- Sono necessarie borse flessibili di grande volume (ad esempio, 250 ml–3 L) laddove gli strumenti BFS sarebbero proibitivi in termini di costi o laddove i contenitori rigidi non sono desiderabili.
- Desideri pellicole multistrato per una migliore barriera all'ossigeno e all'umidità, che può prolungare la durata di conservazione biologica.
Tuttavia, è necessario investire molto in:
- Tecnologia Isolatore/RABS sull'intero percorso di formatura, riempimento e sigillatura.
- Soluzioni validate per la decontaminazione delle pellicole e monitoraggio continuo.
- approfondita del processo Convalida per garantire che nessun residuo sterilizzante interagisca con il biologico. [supporto ]
In breve, FFS può funzionare, ma in genere richiede ingegneria e validazione più complesse per ottenere lo stesso livello di controllo della contaminazione che BFS fornisce in modo più intrinseco. [prestocontatto ]
Quadro pratico di selezione per i produttori biologici
In qualità di fornitore di apparecchiature e integratore di linea, Ningbo Everheal Medical Equipment Co., LTD. può aiutare i clienti a strutturare la decisione sui prodotti biologici termosensibili con un semplice quadro di cinque domande :
1. Quanto è termosensibile il tuo biologico?
- Se il prodotto non tollera la sterilizzazione terminale ed è altamente sensibile al calore, il BFS diventa spesso l'opzione di base più sicura. [vxpbiologics ]
- Per i prodotti moderatamente sensibili, si può comunque prendere in considerazione un FFS asettico avanzato, a condizione che le temperature di sigillatura e l'esposizione agli sterilizzanti rimangano lontane dalle soglie di degradazione. [supporto ]
2. Di quale formato di contenitore ha bisogno la tua terapia?
- Fiale monodose, piccole fiale o prodotti respiratori monodose si allineano naturalmente con BFS . [soluzionisteriliwoodstock ]
- Le borse flessibili di grandi dimensioni o le buste multiscomparto possono favorire il FFS , poiché i sistemi basati su pellicola offrono una maggiore flessibilità geometrica. [rommelag ]
3. Quale livello di rischio di contaminazione puoi accettare?
- I prodotti biologici di alto valore con un basso volume di lotti e un elevato impatto clinico per dose solitamente giustificano la BFS, perché il costo di un evento di contaminazione è inaccettabile. [prestocontatto ]
- Le soluzioni ad alto volume e con margine inferiore possono accettare un rischio FFS ben controllato se supportate da una forte tecnologia di barriera e da un monitoraggio. [rommelag ]
4. Quanto è matura la vostra infrastruttura asettica?
- Un sito senza esperienza in materia di isolatori ma disposto a investire in una linea BFS autonoma può accelerare il go-live con meno complessità. [linkedin ]
- I siti con squadre di isolatori esperte e un forte monitoraggio ambientale possono sfruttare tale competenza per gestire in modo efficiente le linee FFS asettiche. [rommelag ]
5. Qual è il tuo piano di scalabilità e ciclo di vita?
- BFS offre un'eccellente scalabilità per ad alta velocità e ad alto volume . il confezionamento di prodotti biologici liquidi [apigetto ]
- FFS supporta strategie multiprodotto in cui potresti voler riempire liquidi, polveri e prodotti combinati sulla stessa linea nel tempo. [linkedin ]
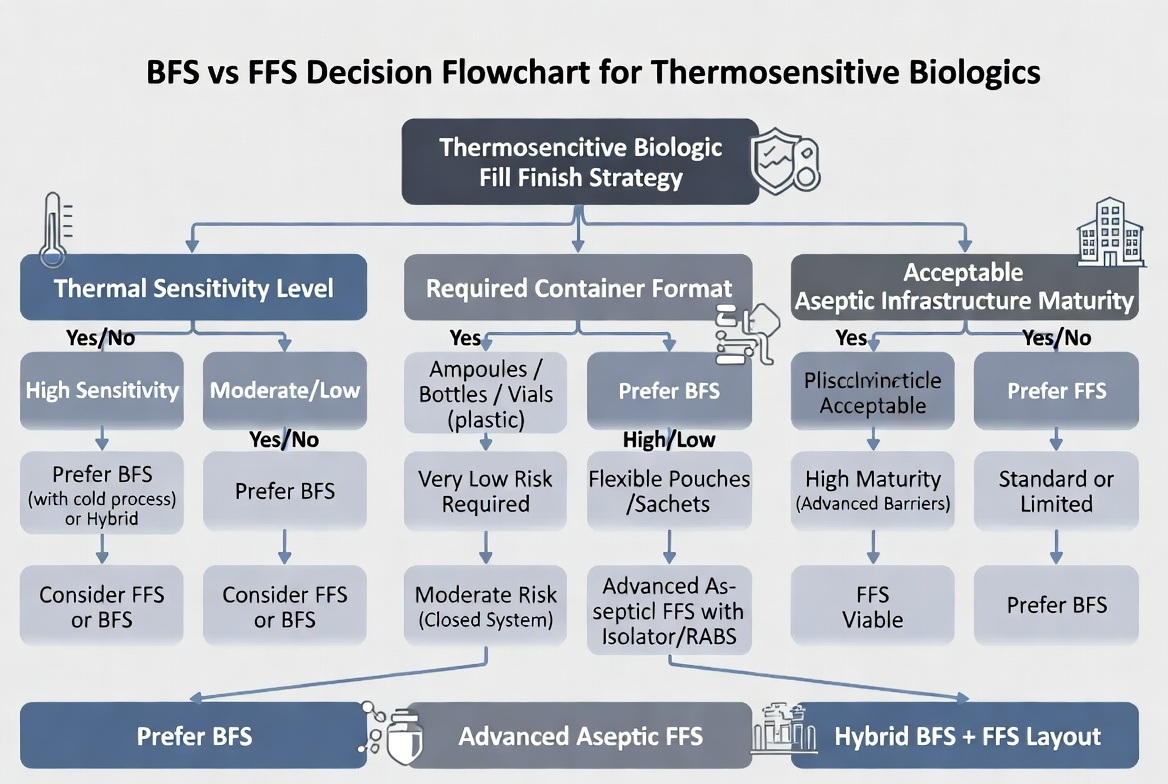
Suggerimenti per l'implementazione degli esperti dal punto di vista dell'ingegneria di linea
Basandosi sui tipici progetti BFS e FFS forniti ai clienti del settore farmaceutico, esistono diversi passaggi pratici per ridurre ulteriormente il rischio di contaminazione, indipendentemente dalla tecnologia scelta.
Consigli di progettazione per le linee BFS
- Progettare la suite BFS con flussi di personale e materiali unidirezionali , riducendo al minimo le opportunità di contaminazione incrociata tra zone pulite e meno pulite. [soluzionisteriliwoodstock ]
- Combina BFS con l'ispezione automatizzata in linea (test visivo e di tenuta) per rilevare tempestivamente problemi di tenuta microscopica o particelle. [apigetto ]
- Standardizzare resine prequalificate e controllare attentamente la manipolazione della resina per evitare contaminazione particellare o microbica prima dell'estrusione. [prestocontatto ]
Suggerimenti ingegneristici per le linee FFS
- Posizionare l'intero percorso di formatura e riempimento all'interno di un isolatore o RABS con controllo della pressione indipendente, non solo nella stazione di riempimento. [supporto ]
- Integrare la decontaminazione online delle pellicole e monitorare continuamente la concentrazione dello sterilizzante e il tempo di esposizione. [rommelag ]
- Utilizzare la zonizzazione basata sul rischio per garantire che gli interventi, la manutenzione e il campionamento non compromettano mai le aree asettiche di massimo livello. [supporto ]
Per i clienti di Ningbo Everheal, un approccio progettuale integrato, che copre la progettazione del layout, la strategia HVAC e la configurazione della linea, spesso ha un impatto maggiore sui tassi di contaminazione nel mondo reale rispetto alla sola scelta tra BFS e FFS. [soluzionisteriliwoodstock ]
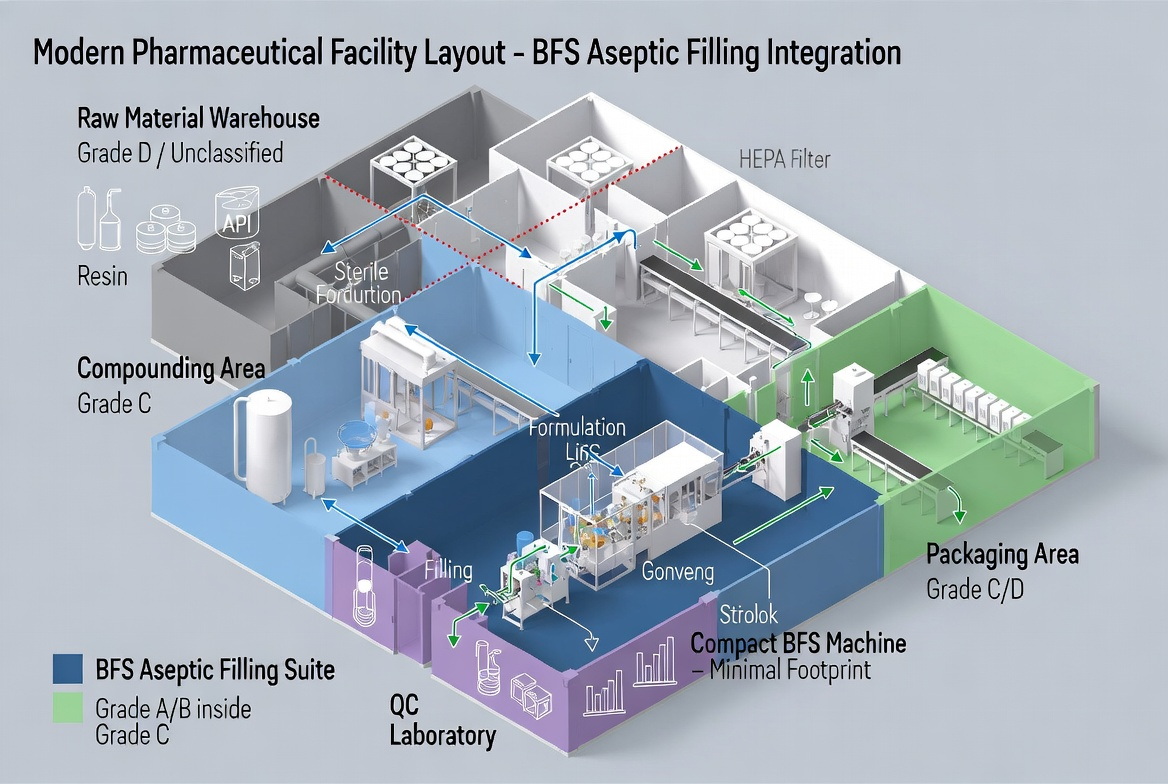
Conclusione: quale tecnologia riduce al minimo i rischi di contaminazione per i prodotti biologici termosensibili?
Dalla letteratura e dall’esperienza a livello di impianto, BFS offre generalmente il rischio di contaminazione intrinseca più basso per i prodotti biologici termosensibili, grazie al suo processo di formatura chiuso, automatizzato, ad alta temperatura e a tempi di esposizione molto brevi. Una linea FFS ben progettata può raggiungere prestazioni asettiche elevate, ma di solito richiede una tecnologia di barriera, fasi di decontaminazione e sforzi di validazione più complessi per raggiungere un profilo di rischio simile. [linkedin ]
Per i produttori che valutano una nuova capacità di riempimento-finitura, la strategia più solida è quella di partire dal profilo di rischio termico e di contaminazione del prodotto biologico , quindi progettare insieme il layout della fabbrica e la configurazione BFS/FFS, piuttosto che considerare le apparecchiature come una decisione a sé stante. È proprio qui che un partner come Ningbo Everheal Medical Equipment Co., LTD., che combina l'esperienza nelle apparecchiature BFS e FFS con la pianificazione del layout della fabbrica, può ridurre il rischio del progetto e il time-to-market. [vxpbiologics ]
Domande frequenti
1. Il BFS è sempre migliore del FFS per i farmaci biologici?
Non sempre. BFS generalmente offre un rischio di contaminazione inferiore, ma per alcuni formati di confezioni speciali o di grandi volumi, una linea FFS asettica con una forte tecnologia di barriera può comunque essere la soluzione migliore. [prestocontatto ]
2. BFS può gestire formulazioni biologiche altamente viscose?
I moderni sistemi BFS possono dosare un'ampia gamma di viscosità, ma viscosità estreme possono richiedere pompe, ugelli e regolazioni del tempo di ciclo specializzati per mantenere la precisione di riempimento e la sterilità. [vxpbiologics ]
3. I contenitori BFS sono compatibili con lo stoccaggio a catena del freddo?
SÌ. I tipici polimeri BFS come LDPE e PP sono compatibili con condizioni refrigerate e molti prodotti biologici confezionati BFS sono progettati per la distribuzione nella catena del freddo. La convalida è ancora richiesta per ogni prodotto specifico. [prestocontatto ]
4. Come vedono le linee guida normative BFS e FFS?
Gli enti regolatori riconoscono il BFS come un processo asettico avanzato con una solida esperienza nei prodotti farmaceutici sterili, mentre il FFS è accettato se supportato da solide validazioni, sistemi di barriera e strategie di controllo della contaminazione. [apigetto ]
5. Qual è la tempistica tipica di implementazione di una nuova linea BFS?
A seconda della personalizzazione e della preparazione della struttura, l'implementazione completa, da URS a PQ, spesso varia da 12 a 24 mesi, compresa la fabbricazione delle apparecchiature, l'installazione, la convalida e la formazione del personale. [soluzionisteriliwoodstock ]
Riferimenti
1. Prestocontatto. 'Qual è la differenza tra il sigillo Blow Fill (BFS) e il sigillo Form Fill (FFS)?' 2025. [Collegamento ]. [prestocontatto ]
2. Shraddha Shinde. 'Tecnologia Blow Fill Seal: garantire la conformità sterile.' LinkedIn, 2025. [Collegamento ]. [linkedin ]
3. Prodotti biologici VxP. 'Sigillo di riempimento ad aria compressa.' 2018. [Collegamento ]. [vxpbiologics ]
4. Rommelag. 'Sigillo di riempimento del modulo: riempimento asettico di prodotti farmaceutici.' 2026. [Collegamento ]. [rommelag ]
5. ApiJect. 'L'evoluzione e i vantaggi della tecnologia Blow-Fill-Seal nel settore farmaceutico.' 2024. [Collegamento ]. [apigetto ]
6. Supporto SU. 'Riempimento asettico e lavorazione di prodotti biologici.' 2024. [Collegamento ]. [supporto ]
7. Sunil Amin. 'FFS e BFS: tecnologie di confezionamento per prodotti farmaceutici.' LinkedIn, 2025. [Collegamento ]. [linkedin ]
8. Soluzioni sterili Woodstock. 'Soluzioni avanzate di produzione asettica.' [Collegamento ]. [soluzionisteriliwoodstock ]






















































